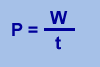3.1 TRANSFORMACIONES DE LA ENERGÍA
|
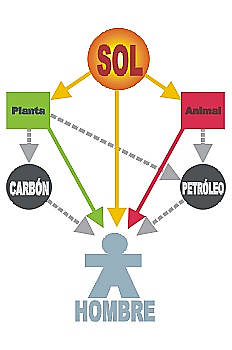
La Energía se encuentra en constante transformación, pasando de unas formas a otras. La energía siempre pasa de formas más útiles a formas menos útiles. Por ejemplo, en un volcán la energía interna de las rocas fundidas puede transformarse en energía térmica produciendo gran cantidad de calor; las piedras lanzadas al aire y la lava en movimiento poseen energía mecánica; se produce la combustión de muchos materiales, liberando energía química; etc.
|
 |
3.2 PRINCIPIO DE CONSERVACIÓN DE LA ENERGÍA
|
El Principio de conservación de la energía indica que la energía no se crea ni se destruye; sólo se transforma de unas formas en otras. En estas transformaciones, la energía total permanece constante; es decir, la energía total es la misma antes y después de cada transformación.
|
En el caso de la energía mecánica se puede concluir que, en ausencia de rozamientos y sin intervención de ningún trabajo externo, la suma de las energías cinética y potencial permanece constante. Este fenómeno se conoce con el nombre de Principio de conservación de la energía mecánica.
|
3.3 DEGRADACIÓN DE LA ENERGÍA
| |||||||||
Unas formas de energía pueden transformarse en otras. En estas transformaciones la energía se degrada, pierde calidad. En toda transformación, parte de la energía se convierte en calor o energía calorífica.
| |||||||||
Cualquier tipo de energía puede transformarse íntegramente en calor; pero, éste no puede transformarse íntegramente en otro tipo de energía. Se dice, entonces, que el calor es una forma degradada de energía. Son ejemplos:
| |||||||||
| |||||||||
Se define, por tanto, el Rendimiento como la relación (en % por ciento) entre la energía útil obtenida y la energía aportada en una transformación.
| |||||||||

| |||||||||
ENERGÍA DE LA BIOMASA
|
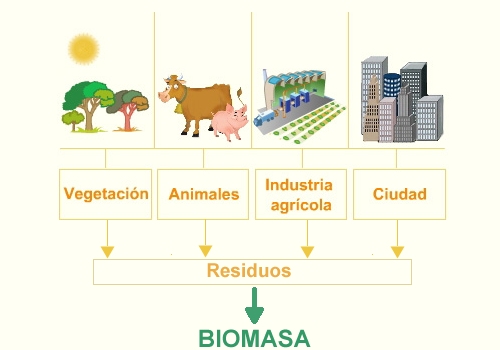
La Energía de la biomasa es la que se
obtiene de los compuestos orgánicos mediante procesos naturales. Con el término
biomasa se alude a la energía solar, convertida en materia orgánica por
la vegetación, que se puede recuperar por combustión directa o transformando esa
materia en otros combustibles, como alcohol, metanol o aceite. También se puede
obtener biogás, de composición parecida al gas natural, a partir de desechos
orgánicos.
|
 |
Ventajas: Es una fuente de energía limpia y
con pocos residuos que, además son biodegradables. También, se produce de forma
continua como consecuencia de la actividad humana.
|
Inconvenientes: Se
necesitan grandes cantidades de plantas y, por tanto, de terreno. Se intenta
"fabricar" el vegetal adecuado mediante ingeniería genética. Su rendimiento es
menor que el de los combustibles fósiles y produce gases, como el dióxido de
carbono, que aumentan el efecto invernadero.
|
4.3 FUENTES DE ENERGÍA NO RENOVABLES
|
Las Fuentes de energía no renovables son aquellas que se encuentran de forma limitada en el planeta y cuya velocidad de consumo es mayor que la de su regeneración.
|
| Existen varias fuentes de energía no renovables, como son: |
|
 |